Nacional
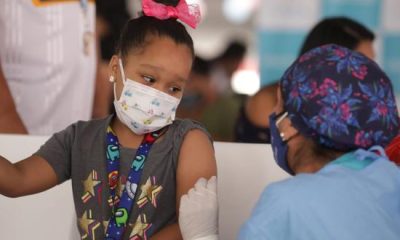
CanSino inicia envasado de 2 millones de dosis de vacuna anti-COVID en Querétaro
El primer lote estará listo en la segunda quincena de marzo y será entregado a la Secretaría de Salud para su distribución y aplicación

Nacional
CFE pone en operación nueva infraestructura para fortalecer la transmisión y transformación de energía eléctrica en la Península de Yucatán
Atenderá el crecimiento de la demanda de las zonas Cancún y Riviera Maya Fase II, con una inversión superior a los $2,156 millones de pesos
Nacional
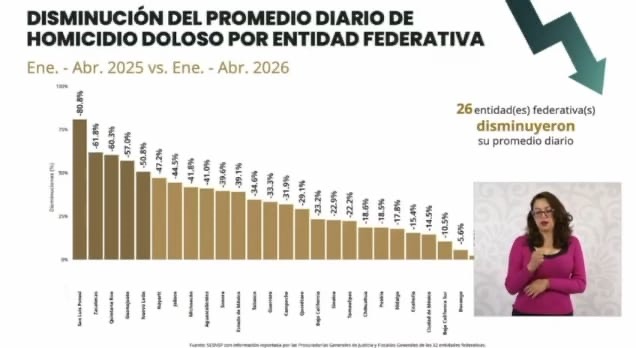
Quintana Roo, el tercer estado con mayor reducción de homicidios dolosos en primer cuatrimestre de 2026
La disminución fue de 60.3% en el primer cuatrimestre de 2026, en comparación al mismo periodo del año anterior
Nacional
Gobierno federal revisará gasolineras por altos precios del diésel; advierten inspecciones a quienes superen los $28.50
Considera que no existe justificación para los precios elevados que actualmente se observan en diversas regiones del país; en Cancún el diésel está por arriba de 28.50 pesos por litro
-

 Turismo
TurismoCaribe Mexicano supera el 70% de ocupación hotelera pese a temporada baja
-

 Afición
AficiónAtlético Quintanarroense conquista el bicampeonato Sub-13 y el título Sub-15 de la Liga Nacional Juvenil
-

 Turismo
TurismoCancún supera 71% de ocupación hotelera en temporada baja; Caribe Mexicano mantiene buena afluencia previo al Mundial 2026
-

 Turismo
TurismoCaribe Mexicano promoverá seis experiencias reconocidas por la UNESCO en Feria Internacional del Mundo Maya
-

 Turismo
TurismoReabren Chichén Itzá tras 13 días de cierre; comunidad maya mantiene lucha por sus derechos
-

 Estado
EstadoMara Lezama invita a celebrar dos años del triunfo de Claudia Sheinbaum en el Malecón Tajamar de Cancún
-

 Estado
EstadoSupervisa Mara Lezama avances en la colocación de la superficie sintética en la primera pista de atletismo certificada de la Península en Chetumal
-

 Estado
EstadoSupervisa Mara Lezama inicio de la conversión de Clínica del ISSSTE de Cancún en Hospital General