Mundo
Aprueban la primera inyección para reducir el riesgo de contraer VIH
Desde el 21 de diciembre, los pacientes con SIDA pueden recibir una inyección intramuscular cada dos meses para reemplazar las tabletas que deben tomar todos los días
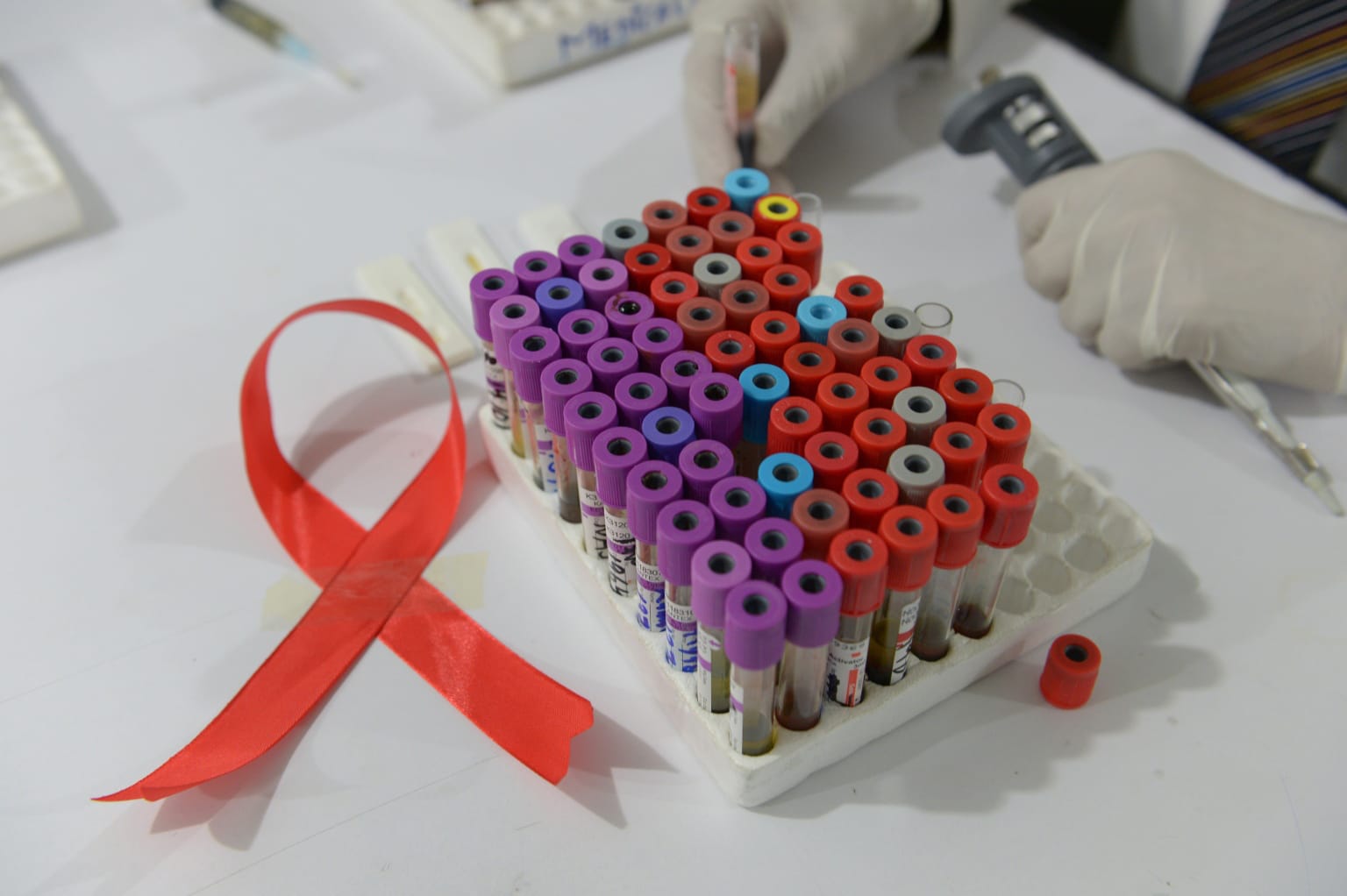
Mundo
Estados Unidos aumenta a 15 mdd la recompensa para capturar a ‘El Mencho’, cofundador del CJNG
El Mencho es cofundador del Cártel Jalisco Nueva Generación
Mundo
Gabriel Boric afirma que fue víctima de acoso sexual, tras denuncia judicial en su contra
El abogado asegura que el gobernante fue víctima de acoso sexual por parte de una mujer hace diez años
Mundo
Cae la primera nevada de la temporada en Pekín
China tiene un sistema de alerta meteorológica de cuatro niveles
-

 Playa del Carmen
Playa del CarmenMayor problema de Playa del Carmen es la movilidad y ocupación del suelo
-

 Afición
AficiónAtlético Quintanarroense Sub-13 cierra con orgullo su participación en la Liga Nacional Juvenil
-

 Nacional
NacionalSe pospone visita de la Presidenta Claudia Sheinbaum a Quintana Roo
-

 Turismo
TurismoViajar está más vivo que nunca: Expedia presenta el Índice del Viajero 2025
-

 Chetumal
ChetumalListo, el plan piloto de transporte urbano en Chetumal
-

 Estado
EstadoMara Lezama entrega obra de rehabilitación de la avenida Miguel Hidalgo de Cancún
-
 Turismo
TurismoQuintana Roo y Airbnb colaboran para impulsar la diversificación turística del Caribe Mexicano: SEDETUR
-

 Playa del Carmen
Playa del CarmenTodavía es pronto para resultados de cambio de nombre de Playa del Carmen
















